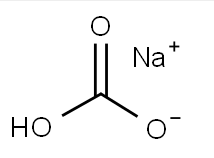
Bicarbonato de sodio CAS#144-55-8
Número CAS:144-55-8
Fórmula química: Atroz
Sinónimos:
QIAN
Fabricante de bicarbonato de sodio
Solución de prueba de bicarbonato de sodio (ChP)
MOQ (cantidad mínima de pedido):1 FCL (carga de contenedor completo)
Apariencia:Líquido transparente incoloro
Bicarbonato de sodio CAS#144-55-8
El bicarbonato de sodio, que es el compuesto comúnmente llamado bicarbonato de sodio, existe como un sólido cristalino blanco e inodoro. Se presenta de forma natural como el mineral nahcolita, que deriva su nombre de su fórmula química al reemplazar el "3" en NaHCO3 con la terminación "lite". La principal fuente mundial de nahcolita es la cuenca de Piceance Creek en el oeste de Colorado, que forma parte de la formación más grande de Green River. El bicarbonato de sodio se extrae mediante minería de solución bombeando agua caliente a través de pozos de inyección para disolver la nahcolita de los lechos del Eoceno, donde se encuentra a 1500 a 2000 pies por debajo de la superficie. El bicarbonato de sodio disuelto se bombea a la superficie, donde se trata para recuperar NaHCO3 de la solución. El bicarbonato de sodio también se puede producir a partir de los depósitos de trona, que son una fuente de carbonatos de sodio (véase Carbonato de sodio).
| Propiedades químicas del bicarbonato de sodio |
| Punto de fusión | >300 °C(lit.) |
| Punto de ebullición | 851 °C |
| densidad aparente | 1000 kg/m3 |
| densidad | 2,16 g/mL a 25 °C (lit.) |
| índice de refracción | 1.500 |
| temperatura de almacenamiento | 2-8°C |
| solubilidad | H2O: 1 M a 20 °C, transparente, incoloro |
| forma | solución (7,5%) |
| color | Blanco |
| Peso específico | 2.159 |
| Olor | Inodoro |
| PH | 8,27 (solución de 1 mM); 8,22 (solución de 10 mM); 8,02 (solución de 100 mM); |
| Rango de pH | 7.8 - 8.2 |
| pka | (1) 6,37, (2) 10,25 (carbónico (a 25℃) |
| Solubilidad en agua | 9 g/100 mL (20 ºC) |
| Descomposición | 50 °C |
| Merck | 14.8583 |
| BRN | 4153970 |
| Clase BCS | 1 |
| Estabilidad: | Estable. |
| Funciones de los ingredientes cosméticos | DESODORANTE BÚFER ABRASIVO CUIDADO BUCAL PROTECCIÓN DE LA PIEL |
| Iniciar sesión | -4.010 (estimado) |
| Referencia de la base de datos CAS | 144-55-8 (Referencia de base de datos CAS) |
| Sistema de Registro de Sustancias de la EPA | Bicarbonato de sodio (144-55-8) |
| Información de seguridad |
| Declaraciones de seguridad | 24/25 |
| WGK Alemania | 1 |
| RTECS | VZ0950000 |
| Ley de Control de Sustancias Tóxicas | Sí |
| Código HS | 28363000 |
| Datos sobre sustancias peligrosas | 144-55-8 (Datos sobre sustancias peligrosas) |
| Toxicidad | LD50 por vía oral en conejos: 4220 mg/kg |
Aplicación del producto de bicarbonato de sodio CAS#144-55-8
El bicarbonato de sodio, utilizado en forma de bicarbonato de sodio y levadura química, es el agente leudante más común. Al añadir bicarbonato de sodio, una sustancia alcalina, a una mezcla, reacciona con un ingrediente ácido para producir dióxido de carbono. La reacción se puede representar como: NaHCO₃(s) + H+ → Na+(ac) + H₂O(l) + CO₂(g), donde el H+ es aportado por el ácido. Los polvos para hornear contienen bicarbonato de sodio como ingrediente principal, junto con ácido y otros ingredientes. Dependiendo de la formulación, los polvos para hornear pueden producir dióxido de carbono rápidamente, como un polvo de acción simple, o en etapas, como un polvo de doble acción. El bicarbonato de sodio también se utiliza como fuente de dióxido de carbono para bebidas carbonatadas y como tampón. Además de la repostería, el bicarbonato de sodio tiene numerosos usos domésticos. Se utiliza como limpiador general, desodorante, antiácido, extintor de incendios y en productos de higiene personal como la pasta de dientes. El bicarbonato de sodio es una base débil en solución acuosa, con un pH aproximado de 8. El ion bicarbonato (HCO₃₂) tiene propiedades anfóteras, lo que significa que puede actuar como ácido o como base. Esto le confiere al bicarbonato de sodio una capacidad amortiguadora y la capacidad de neutralizar tanto ácidos como bases. Los olores de alimentos resultantes de compuestos ácidos o básicos se pueden neutralizar con bicarbonato de sodio en sales inodoras. Al ser una base débil, el bicarbonato de sodio tiene una mayor capacidad para neutralizar los olores ácidos.
El segundo uso más importante del bicarbonato de sodio, que representa aproximadamente el 25% de la producción total, es como suplemento alimenticio agrícola. En el ganado bovino, ayuda a mantener el pH ruminal y facilita la digestibilidad de la fibra; en las aves de corral, ayuda a mantener el equilibrio electrolítico al aportar sodio a la dieta, ayuda a las aves a tolerar el calor y mejora la calidad de la cáscara del huevo.
El bicarbonato de sodio se utiliza en la industria química como agente amortiguador, agente de expansión, catalizador y materia prima química. Se emplea en la industria del curtido de cueros para el pretratamiento y la limpieza de pieles, así como para controlar el pH durante el proceso. El calentamiento del bicarbonato de sodio produce carbonato de sodio, que se utiliza en la fabricación de jabón y vidrio. Se incorpora a productos farmacéuticos como antiácido, agente amortiguador y, en formulaciones, como fuente de dióxido de carbono en tabletas efervescentes. Los extintores de polvo químico tipo BC contienen bicarbonato de sodio (o bicarbonato de potasio). Otros usos del bicarbonato incluyen el procesamiento de pulpa y papel, el tratamiento de aguas y la perforación de pozos petrolíferos.
Feria de fábricas y equipos
Tiempo de entrega rápido
Inventario 2-3 días laborables Nueva producción 7-10 días laborables